|
Федеральная служба по надзору в сфере здравоохранения и социального развития уведомляет, что в связи с выявлением серьезных побочных эффектов при применении инъекционных препаратов гепарина, связанных с наличием в субстанции гепарина примеси гиперсульфатированного хондроитинсульфата (ГСХС), разработаны и предложены две методики идентификации данной примеси - капиллярный электрофорез в капиллярном растворе (зональный капиллярный электрофорез) и 1Н-ЯМР спектроскопия (Прилагается).
Федеральная служба по надзору в сфере здравоохранения и социального развития предлагает держателям регистрационных удостоверений на субстанции гепарина внести в нормативную документацию предложенные методы для проведения экспертизы качества субстанции гепарина по показателю "Посторонние примеси - содержание ГСХС".
Организациям-поставщикам субстанции гепарина и организациям-производителям готовых инъекционных препаратов гепарина предлагается внести соответствующие изменения в спецификации для осуществления входного контроля субстанции гепарина.
Приложение на 9 л в 1 экз.
Врио Руководителя И.Ф. Серегина
Методики идентификации посторонних примесей в субстанциях гепарина
I. Капиллярный электрофорез в свободном растворе (зональный капиллярный электрофорез)
Требование:
На электрофореграмме тестируемого раствора не должен присутствовать остроконечный пик гиперсульфатированного хондроитин сульфата перед пиком гепарина. Допускается наличие пика дерматан сульфата после пика гепарина.
Реактивы:
- Стандартный образец гепарина - Sigma H-3393
- Однозамещенный фосфат натрия, моногидрат - ч.д.а.
- Фосфорная кислота - ч.д.а
- Вода дистиллированная и деионизованная (далее - вода)
Оборудование и материалы
1. Оборудование
Прибор: Agilent 3DCE (Agilent Technologies, Вальдбронн, Германия), программа регистрации и обработки данных Agilent ChemStation, версии от А.08.03 или аналогичный.
Капилляр: Кварцевый немодифицированный с внутренним диаметром 50 мкм, эффективной длиной 56 см, полной длиной 64,5 см - Agilent G1600-62211 или аналогичный.
2. Буферный раствор
Растворить 1,0 г (точная навеска) однозамещенного фосфата натрия моногидрата в 100 мл воды, довести рН до 3,5 с помощью фосфорной кислоты, довести объем водой в мерной колбе до 200 мл.
Используемый для анализа объем буферного раствора отфильтровать через целлюлозно-ацетатный мембранный фильтр с размером пор 0,22 мкм, дегазировать.
3. Раствор стандартного образца гепарина
Приготовить раствор стандартного образца гепарина натрия в концентрации 10 мг/мл в воде, отфильтровать через целлюлозно-ацетатный мембранный фильтр с размером пор 0,22 мкм, дегазировать.
4. Испытуемый раствор
Приготовить раствор гепарина натрия в концентрации 10 мг/мл в воде, отфильтровать через целлюлозно-ацетатный мембранный фильтр с размером пор 0,22 мкм, дегазировать.
Методика
1. Кондиционирование капилляра
Перед началом эксплуатации новый капилляр промыть 1 М раствором NaOH 3 минуты, дважды водой по 10 мин, буферным раствором 15 мин.
Между снятием каждой электрофореграммы кондиционировать капилляр следующим образом:
1 М NaOH - 2 мин при 950 мбар
Вода - дважды из разных емкостей по 3 мин при 950 мбар
Буферный раствор - дважды из разных емкостей по 3 мин при 950 мбар
Выдерживание в буферном растворе - 10 мин без давления
2. Проведение анализа
Введение образца: 10 сек при 50 мбар.
Детектор: 192 нм с шириной полосы 8 нм.
Напряжение: 20 кВ. Отрицательная полярность.
Температура капилляра: 30°С.
Время анализа: 20 мин.
Снимают электрофореграмму стандартного образца гепарина. Затем снимают электрофореграммы испытуемых образцов. Через каждые 5 измерений образцов повторяют снятие электрофореграммы стандарта.
3. Пригодность системы
Абсолютное время удерживания пика стандартного образца гепарина определяется физико-химическими свойствами каждого экземпляра используемого капилляра.
Воспроизводимость времени удерживания стандартного образца гепарина при 5 последовательно снятых на одном капилляре без дополнительных интервалов (кроме кондиционирования) электрофореграммах должна быть не хуже ± 0,1 мин.
Для заключения о наличии примесей время удерживания пиков на каждой электрофореграмме должно различаться не менее чем на 0,3 мин. При различии во времени удерживания пиков менее чем 0,3 мин для их идентификации используют добавление в пробу внутреннего стандарта гепарина; для этого растворы пробы и стандарта гепарина (каждый по 10 мг/мл), смешиваются в объемном отношении 1:1.
Оценка результатов на основе типичных электрофореграмм
А. Типичная электрофореграмма чистого гепарина (стандарта) представлена на рис.1.
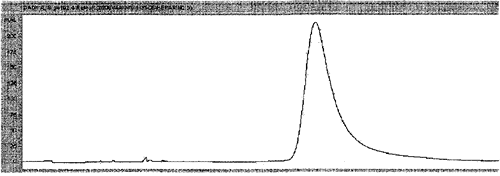
Рис.1 Электрофореграмма чистого гепарина.
Б. В присутствии допустимой примеси дерматан сульфата наблюдается второй пик после гепарина (рис. 2).
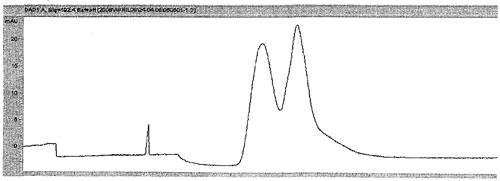
Рис. 2 Электрофореграмма гепарина с примесью дерматансульфата.
В. В присутствии гиперсульфатированного хондроитинсульфата наблюдается остроконечный пик перед гепарином, который в данном случае проявляется в виде неразделенного пика или плеча справа от хондроитинсульфата (рис. 3).
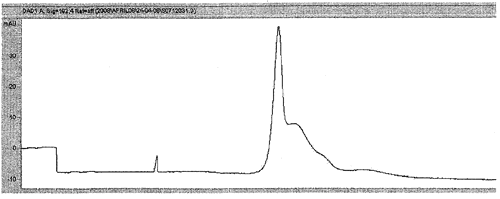
Рис. 3 Электрофореграмма гепарина с примесью гиперсульфатированного хондроитинсульфата.
Г. Электрофореграмма с тремя неразделенными пиками свидетельствует о присутствии в пробе в качестве примесей как дерматансульфата, так и гиперсульфатированного хондроитинсульфата (рис. 4).
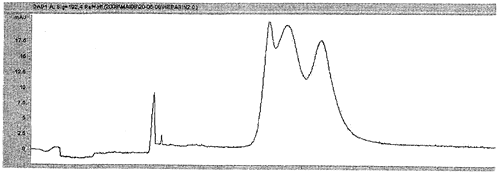
Рис. 4 Электрофореграмма гепарина (центральный пик) с примесями дерматансульфата (справа от гепарина)
и гиперсульфатированного хондроитинсульфата (слева от гепарина)
II. 1H-ЯМР спектроскопия
Требование:
В диапазоне 1,5-2,5 м.д. не допускается присутствие характерного для гиперсульфатированного хондроитин сульфата сигнала при 2,16±0,03 м.д. Допускается наличие пика дерматан сульфата при 2,08±0,03 м.д.
Реактивы:
- USP Heparin Sodium Identification RS
- USP Heparin Sodium System Suitability RS
- оксид дейтерия
Оборудование и материалы
1. Оборудование
Импульсный ЯМР Фурье-спектрометр с рабочей частотой на протонах 200 МГц и более.
2. Раствор стандартного образца гепарина
12 мг USP Heparin Sodium Identification RS переносят в 5 мм ампулу для ЯМР и растворяют в 1 мл оксида дейтерия.
3. Раствор пригодности системы
12 мг USP Heparin Sodium System Suitability RS переносят в 5 мм ампулу для ЯМР и растворяют в 1 мл оксида дейтерия.
4. Испытуемый раствор
60 мг исследуемого гепарина переносят в 5 мм ампулу для ЯМР и растворяют в 1 мл оксида дейтерия.
Методика
Температура: 25°С.
Ширина спектрального диапазона: 10 м.д.
AQ: 4,096
Время задержки между сканированиями (RD): не менее 1,0 сек.
Регистрируют спектр стандартного образца гепарина. Затем регистрируют спектры испытуемых образцов.
Количество сканирований определяется по достижению величины отношения сигнал/шум значения 200 у сигнала N-ацетильных протонов гепарина (2,04 м.д.) в стандартном растворе.
Величины химических сдвигов сигналов в спектрах гепарина относят по наиболее сильнопольному сигналу, расположенному в области 2,04 м.д. в спектре стандартного раствора гепарина, и соответствующему N-ацетильным протонам гепарина.
Химические сдвиги для гепарина и гиперсульфатированного хондроитин сульфата в спектре раствора пригодности системы равны 2,04±0,02 и 2,16±0,03 м.д. соответственно. Спектр испытуемого раствора регистрируют при условиях записи, аналогичных стандартному раствору. N-ацетильные протоны гепарина должны показывать основной сигнал при 2,04±0,02 м.д. Сигнал, соответствующий N-ацетильным протонам дерматана сульфата, может быть выявлен в области 2,08 м.д. Наблюдение резонанса при 2,16±0,03 м.д. свидетельствует о присутствии гиперсульфатированного хондроитина сульфата. Гиперсульфатированный хондроитина сульфат не имеет других резонансов в области 2,12-3,00 м.д.
Оценка результатов на основе типичных ЯМР-спектров
А) Типичный спектр чистого гепарина (стандарта) представлен на рис. 5.
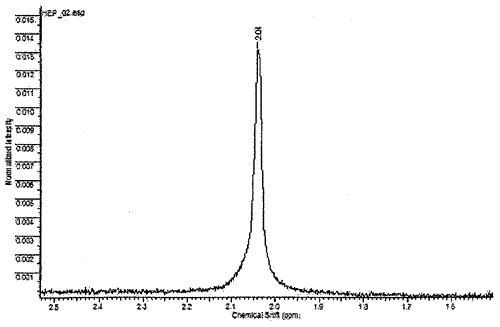
Рис. 5 Спектр чистого гепарина - пик только при 2,04 м.д.
Б) В присутствии допустимой примеси дерматан сульфата наблюдается дополнительный пик 2,08±0,02 м.д. (рис. 6).
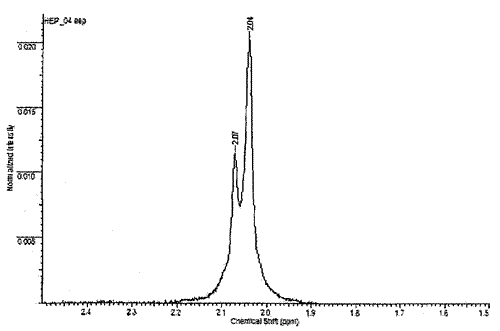
Рис. 6 Спектр гепарина с примесью дерматан сульфата.
В) В присутствии гиперсульфатированного хондроитинсульфата наблюдается дополнительный пик при 2,16±0,03 м.д. (рис. 7).
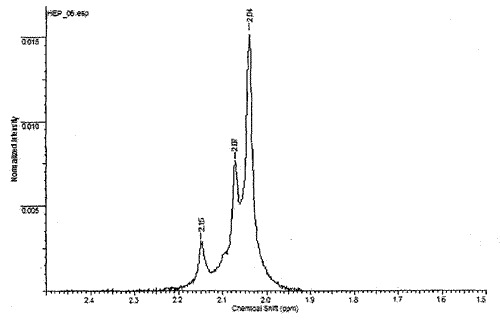
Рис.7 Спектр гепарина (2,04±0,03 м.д.) с примесями дерматан сульфата (2,08±0,03 м.д.)
и гиперсульфатированного хондроитинсульфата (2,16±0,03 м.д.)
|